江苏省药理学会抗炎免疫药理专委会主任委员、南京大学孙洋教授和江苏省药理学会副理事长、南京大学徐强教授研究团队在强直性脊柱炎发病机制和疾病动物模型建立领域取得重要进展,提出异常软骨内骨化是强直性脊柱炎异位骨赘形成的直接原因,使用Smo抑制剂Sonidegib靶向软骨可显著阻止强直性脊柱炎的骨融合进程。研究成果以“Targeting chondrocytes for arresting bony fusion in ankylosing spondylitis”(靶向软骨细胞阻止强直性脊柱炎骨融合)为题,于2021年11月11日在Nature Communications(《自然·通讯》)上在线发表,论文链接:https:// www.nature.com/articles/s41467-021-26750-6。

强直性脊柱炎(Ankylosing spondylitis, AS)号称“不死的癌症”,是一种以脊柱为主要病变部位的自身免疫性疾病,并可累及骶髂关节,引起脊柱强直。与类风湿关节炎等疾病不同,AS患者炎症与骨侵蚀进展时伴随着异位骨化。当异位骨化形成的骨赘充斥关节腔,进而将关节中两端骨连接可致关节僵硬、脊柱强直和脊柱变形,甚至形成“折叠人”。炎症一直被认为是AS异位骨化的诱因,现有AS治疗药物如非甾体类抗炎药、anti-TNF-α单抗可快速减轻炎症与疼痛,但却不能明显阻止AS患者的骨病变进展。
孙洋/徐强团队在一次偶然的机会发现CD4-Cre介导的SHP2条件性敲除小鼠7月龄以上会出现脊柱、髋关节和骶髂关节等中轴关节变形与僵直症状。Micro-CT分析显示在7月龄后CD4-Cre;SHP2f/f(CD4-CKO)小鼠异位骨化形成骨赘逐渐充斥关节腔并铰链两端骨,导致关节僵直,小鼠12月龄时脊柱、骶髂关节、髋关节和膝关节等大关节均出现骨融合和关节僵直,小鼠活动艰难。研究人员进而对小鼠自发骨病变的原因进行了探究。通过T细胞转输、骨髓移植以及使用Lck-Cre;SHP2f/f小鼠等实验证实T细胞和其他免疫细胞并不是CD4-Cre;SHP2f/f小鼠骨病变的诱因。使用mTmG荧光示踪技术发现CD4-Cre还介导了一群软骨细胞中SHP2的敲除。SHP2缺失促进软骨细胞增殖分化,导致小鼠骨骺生长板以及起止点等位置软骨细胞异常增殖并分泌BMP6等蛋白促进成骨细胞分化,加剧异位骨化形成。在CD4-Cre;SHP2f/f小鼠发病早期给予Smo抑制剂Sonidegib可显著抑制小鼠异位骨化和骨融合的症状(图1)。
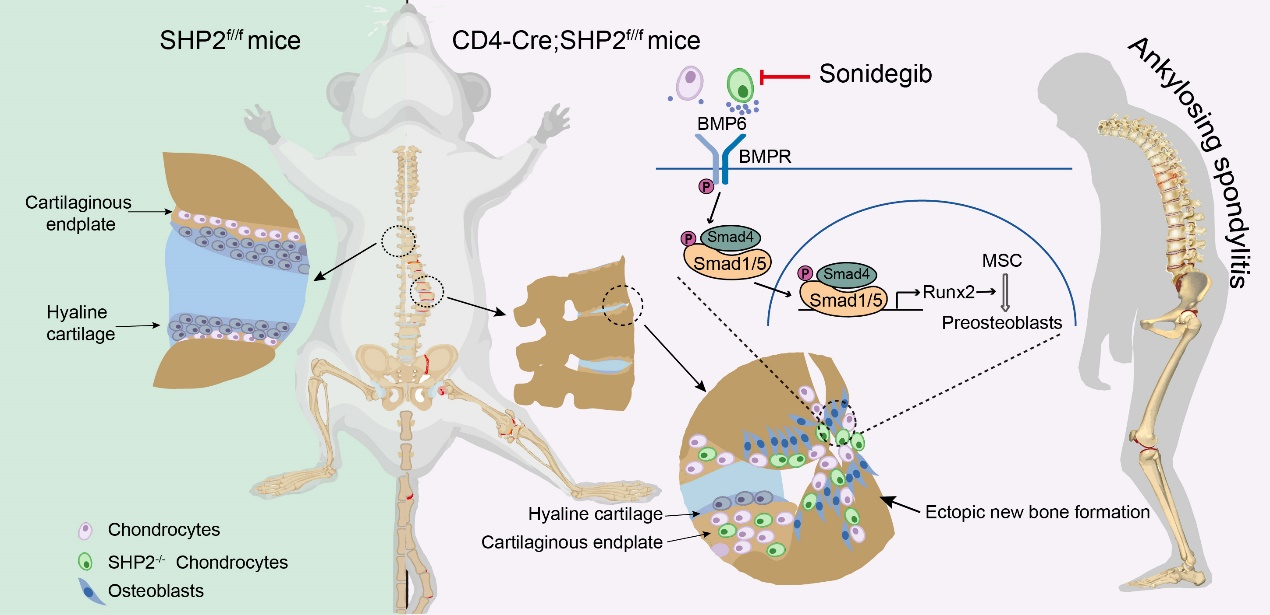
长期以来,由于难以从患者脊柱关节获取组织,以及缺乏贴近临床表型的理想动物模型,强直性脊柱炎的发病机制研究举步维艰。孙洋、徐强团队通过偶然发现的CD4-Cre条件性敲除SHP2的小鼠出现自发强直样表型(骨变形、骨赘、骨质疏松和骨融合),并以此小鼠为模型揭示了生长板闭合延迟是强直性脊柱炎发病的一种崭新机制,CD4-Cre条件性敲除SHP2的小鼠可作为一种新的探究强直性脊柱炎发病机制、干预靶标以及药物研发的理想实验动物模型。
综上所述,该研究揭示了强直性脊柱炎的骨赘是由软骨内成骨所形成,靶向软骨细胞Hedgehog信号可直接抑制软骨内成骨过程的源头,从而显著改善强直性脊柱炎的骨病变进展。值得一提的是,该研究发现通过给予临床老药Sonidegib可抑制新骨形成延缓强直性脊柱炎的骨病变进展,为强直性脊柱炎的治疗提供了一种新的策略,具有潜在的临床应用价值。

